衡水金卷先享题 2021-2022学年度高三一轮复习摸底测试卷[新高考·重庆] 化学(三)3答案

衡水金卷先享题 2021-2022学年度高三一轮复习摸底测试卷[新高考·重庆] 化学(三)3答案,目前我们已经整理了衡水金卷先享题 2021-2022学年度高三一轮复习摸底测试卷[新高考·重庆] 化学(三)3答案的各科答案和试卷,更多试卷答案请关注本答案网。
![衡水金卷先享题 2021-2022学年度高三一轮复习摸底测试卷[新高考·重庆] 化学(三)3答案 衡水金卷先享题 2021-2022学年度高三一轮复习摸底测试卷[新高考·重庆] 化学(三)3答案](https://751p.oss-cn-hongkong.aliyuncs.com/2022/03/7946028318428911915.jpg)

2.答案A命题透析本题考查化学用语,意在考查对中学化学基础知识融会贯通的能力。思路点拨O●是甲烷的球棍模型,A项错误;乙醇的结构简式为CH1CH2OH,BO=C-0,C项正确;用此方法获取液体燃料有望缓解目前的能源危机,D项正确
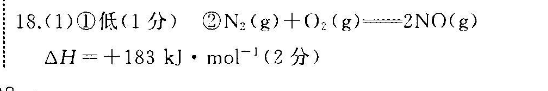


18.(1)①低(1分)②N2(g)+O)2(g)=2NO(g)△H=+183kJ·mol-(2分)(2)①>(1分)②使用催化剂(1分)=(1分)③△H2=2△H1+6△H2[或△H1=(△H2-6△H3)或△H3=(△H2-2△H1)](2分)(2)TiCI (g)+2C0(g)=TiO (s)+2Cl2(g)+2C(s)△H=+45.5kJ·mo1-(2分)②>(1分)【解析】(1)①根据图示可知反应物断键吸收的能量为945kJ+498kJ=1443kJ.生成生成物化学键放出的能量为2×630kJ=1260kJ.吸收的能量大于放出的能量,为吸热反应,则1molO2与1molN2的总能量比2 mol No的总能量低。②反应热为1443kJ·mol-11260kJ·mol-=+183kJ·mol-,则热化学方程式为N2(g)+O2(g)=2NO(g)△H=+183kJ·mol-(2)①通过图中信息可判断反应物总能量小于生成物总能量,属于吸热反应,因此△H1>0。②图中途径Ⅱ的活化能降低,因此条件是使用催化剂,由于催化剂不能改变反应热,则途径I的反应热=途径Ⅱ的反应热。③根据盖斯定律可知(-2×|)×即得到H:(g)+oO(g)H: O(g) AH(△H22△H1)。(3)①利用盖斯定律,将I-Ⅱ,便可得出TCl(g)2CO(g)- TiO,(s)+ 2Ch,(g)+2C(s)AH+45.5kJ·mo1-1。②因为活化能E(正反应)-E(逆反应)=△H,所以若反应Ⅱ的逆反应活化能表示为EkJ·mol1,则E(逆反应)=E(正反应)-△H>220.9。





