尚文原创 2023届云南名校高考适应性月考试卷(二)2语文试题答案

尚文原创 2023届云南名校高考适应性月考试卷(二)2语文试题答案,目前我们已经整理了尚文原创 2023届云南名校高考适应性月考试卷(二)2语文试题答案的各科答案和试卷,更多试卷答案请关注本答案网。

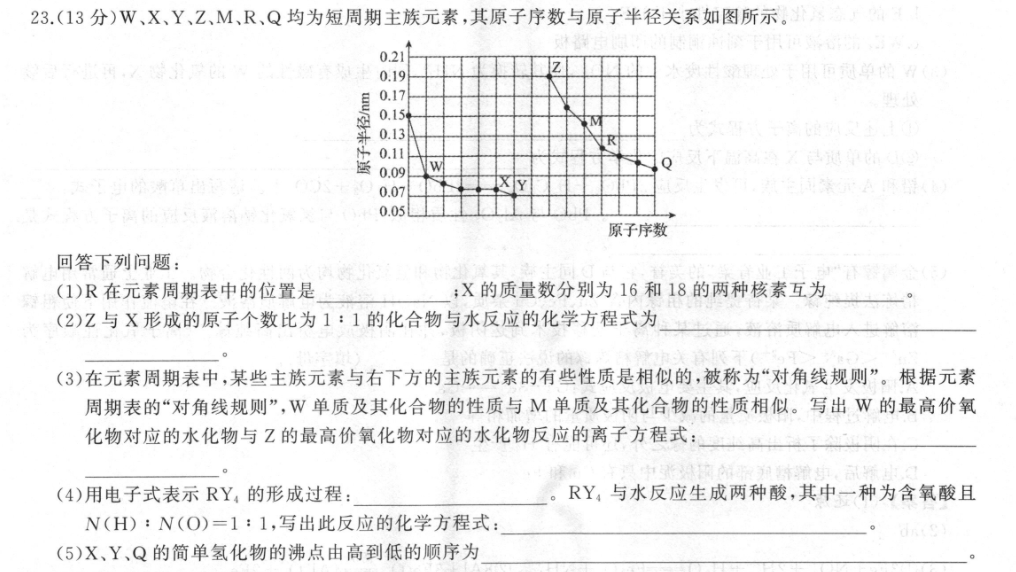


23.(13分)W、X、Y、Z、M、R、Q均为短周期主族元素,其原子序数与原子半径关系如图所示。0.210.190.170.150.13R0.110.09WQ0.07区y0.05原子序数回答下列问题:(1)R在元素周期表中的位置是:X的质量数分别为16和18的两种核素互为(2)Z与X形成的原子个数比为1:1的化合物与水反应的化学方程式为(3)在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的,被称为“对角线规则”。根据元素周期表的“对角线规则”,W单质及其化合物的性质与M单质及其化合物的性质相似。写出W的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物反应的离子方程式:(4)用电子式表示RY,的形成过程:RY4与水反应生成两种酸,其中一种为含氧酸且N(H):N(O)=1:1,写出此反应的化学方程式:(5)X、Y、Q的简单氢化物的沸点由高到低的顺序为【答案】(1)第三周期第VA族(2分)同位素(1分)(2)2Na2O2+2H204NaOH+O2↑(2分)(3)Be(OH)2+20H-BeO+2H2O(2):兴是干步其心是天用的上【形照(4)4:E·+i→::Si::(2分)SiF,+4H,0—H,SiO,+4HF(2分):F:(5)H2O>HF>HCI(2分)【解析】根据关系图可推知W、X、Y、Z、M、R、Q分别为Be元素、O元素、F元素、Na元素、Al元素、Si元素、CI元素。(I)S元素在元素周期表中的位置是第三周期第VNA族;质子数相同,中子数不同的核素互为同位素,O的质量数分别为16和18的两种核素互为同位素。(2)Z为Na元素,X为O元素,二者形成的原子个数比为1:1的化合物为Na2O2,与水反应的化学方程式为2Na2O2+2H2O-4NaOH+O2↑。(3)W为Be元素,M为Al元素,Z为Na元素,由Be与Al单质及其化合物的性质相似,则Be(OH)2与NaOH反应的离子方程式为Be(OH)2+2OH—BeO十2H2O。:斑(4)Y为F元素,R为Si元素,用电子式表示RY4的形成过程为4:+i→::Si::;SiF4与水反应生成两种酸,:F:其中一种为含氧酸且N(H):N(O)=1:1,推知其为HSiO,则另一种酸为HF,此反应的化学方程式为SiF4+4H2O-H,SiO4¥+4HF。(5)X、Y、Q的简单氢化物分别为H2O、HF、HCI。H2O、HF分子之间存在氢键,沸,点均比HCI的沸,点高,又因为常温下H2O为液体,HF为气体,X、Y、Q的简单氢化物的沸点由高到低的顺序为H2O>HF>HCI。
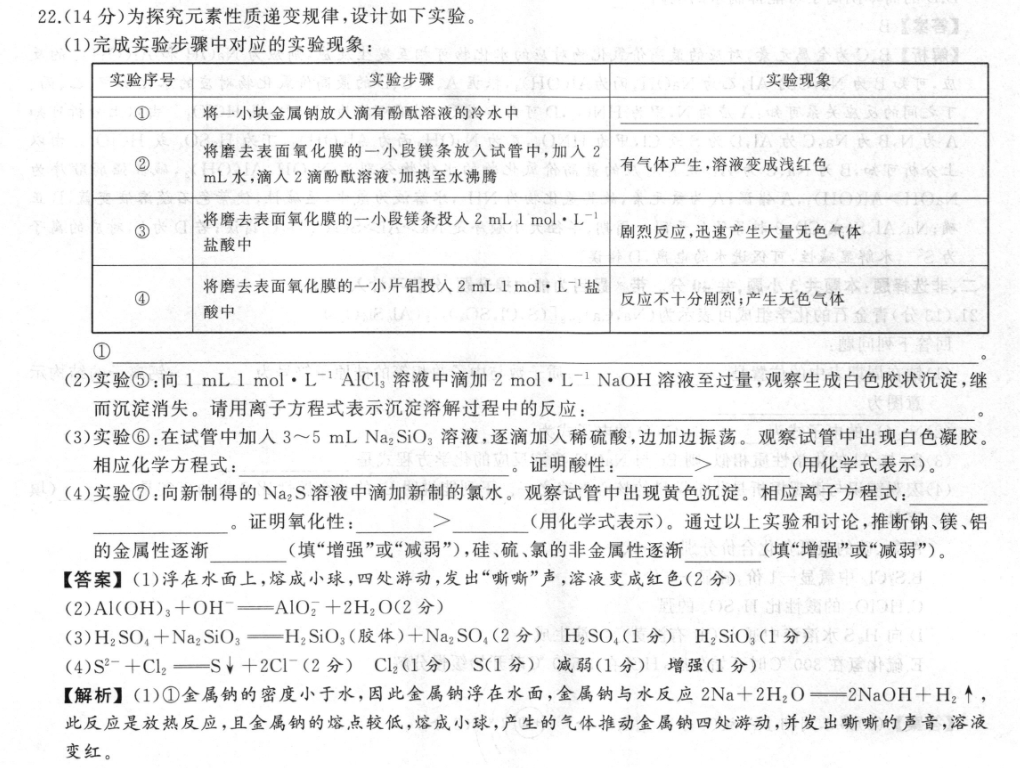

22.(14分)为探究元素性质递变规律,设计如下实验。案容(1)完成实验步骤中对应的实验现象:实验序号实验步骤实验现象①将一小块金属钠放入滴有酚酞溶液的冷水中将磨去表面氧化膜的一小段镁条放入试管中,加入2②有气体产生,溶液变成浅红色mL水,滴入2滴酚酞溶液,加热至水沸腾将磨去表面氧化膜的一小段镁条投入2mL1mol·L③剧烈反应,迅速产生大量无色气体A/盐酸中将磨去表面氧化膜的一小片铝投入2mL1mol·L'盐④反应不十分刷烈:产生无色气体酸中金青(谷)1图①(2)实验⑤:向1mL1mol·L-1A1Cl3溶液中滴加2mol·L-1NaOH溶液至过量,观察生成白色胶状沉淀,继而沉淀消失。请用离子方程式表示沉淀溶解过程中的反应:(3)实验⑥:在试管中加入3~5mLNa2SiO3溶液,逐滴加人稀硫酸,边加边振荡。观察试管中出现白色凝胶。相应化学方程式:的。证明酸性:>(用化学式表示)。(4)实验⑦:向新制得的Na2S溶液中滴加新制的氯水。观察试管中出现黄色沉淀。相应离子方程式:。证明氧化性:>(用化学式表示)。通过以上实验和讨论,推断钠、镁、铝的金属性逐渐(填“增强”或“减弱”),硅、硫、氯的非金属性逐渐合(填“增强”或“减弱”)。【答案】(1)浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,溶液变成红色(2分)显(2)A1(OH)3+OH—A1O2+2H2O(2分)(3)H2SO4+Na2SiO3—H2SiO3(胶体)+Na2SO4(2分)H2SO,(1分)H2SiO3(1分)太21(4)S2-+C12—S¥+2C1-(2分)Cl2(1分)S(1分)减弱(1分)1增强(1分)0008。【解析】(1)①金属钠的密度小于水,因此金属钠浮在水面,金属钠与水反应2Na+2H2O一2NaOH+H2个,此反应是放热反应,且金属钠的熔点较低,熔成小球,产生的气体推动金属钠四处游动,并发出嘶嘶的声音,溶液变红。(2)生成白色胶状沉淀A13+十3OH一A1(OH)3¥,因为氢氧化铝表现两性,能与氢氧化钠反应,因此沉淀溶解的离子方程式为A1(OH)3+OH一AIO2+2H2O。(3)白色凝胶是H2SiO3,反应的化学方程式为Na2SiO3+H2SO,-Na2SO4+H2SiO3(胶体),利用强酸制取弱酸的原理,因此酸性H2SO,>H2SiO3。(4)黄色沉淀是S,发生H2S十CI2一2HC十S¥,氧化剂的氧化性大于氧化产物的氧化性,即氧化性Cl2>S;钠能与冷水反应,Mg与热水反应,因此Na的金属性强于Mg,Mg与盐酸反应剧烈,AI与盐酸反应不剧烈,说明Mg的金属性强于Al,因此N、Mg、AI的金属性依次减弱;非金属性越强,其最高价氧化物的水化物酸性越强,即非金属性S>Si,氧化剂的氧化性大于氧化产物的氧化性,即CI的非金属性强于S,因此Si、S、CI的非金属性依次增强。





